鉻明礬[KCr(SO4)2?12H2O]易溶于水�����,難溶于乙醇�����,主要用作鞣劑���,媒染劑及照相定影劑等。某實(shí)驗(yàn)小組通過SO2還原K2Cr2O7酸性溶液來制備����,其裝置如圖所示:
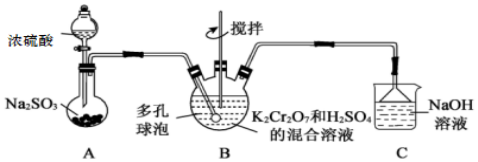
(1)寫出A中發(fā)生的化學(xué)反應(yīng)方程式
Na2SO3+H2SO4(濃)=Na2SO4+SO2↑+H2O
Na2SO3+H2SO4(濃)=Na2SO4+SO2↑+H2O
。
(2)裝置B中K2Cr2O7所發(fā)生反應(yīng)的離子反應(yīng)方程式為 Cr2O72-+2H++3SO2=2Cr3++3SO42-+H2O
Cr2O72-+2H++3SO2=2Cr3++3SO42-+H2O
����;其中多孔球泡的作用是 使SO2吸收完全
使SO2吸收完全
。
(3)裝置B中充分反應(yīng)后�,獲得鉻明礬晶體的方法:向混合物中加入乙醇后析出晶體,經(jīng)過 過濾�、洗滌
過濾、洗滌
�����,干燥后得到鉻明礬晶體,向裝置B的混合物中加入乙醇的目的是 降低鉻鉀釩在水中的溶解量
降低鉻鉀釩在水中的溶解量
��。
(4)測定樣品純度:
步驟一:稱取1.000g產(chǎn)品配成250mL溶液��,取25.00mL溶液于錐形瓶中�;
步驟二:加適量NaOH將其轉(zhuǎn)化為CrO2-��,并加稍過量的H2O2將CrO2-氧化為CrO42-�;
步驟三:再加入過量的H2SO4酸化并煮沸,加入足量的KI固體�����,加塞搖勻���,將Cr(VI)還原為Cr3+����;
步驟四:加入適量淀粉溶液���,用0.02000mol/LNa2S2O3標(biāo)準(zhǔn)溶液滴定至終點(diǎn)�����,平行測定三次��,平均消耗Na2S2O3標(biāo)準(zhǔn)溶液24.00mL(已知:2Na2S2O3+I2═Na2S4O6+2NaI)���。
①加入硫酸后CrO42-發(fā)生的離子反應(yīng)方程式為 2CrO42-+2H+═Cr2O72-+H2O
2CrO42-+2H+═Cr2O72-+H2O
����;
②步驟三中加入KI固體前要將溶液加熱煮沸����,其主要原因是 除去溶解的氧氣,防止氧氣氧化碘離子���,產(chǎn)生誤差
除去溶解的氧氣�����,防止氧氣氧化碘離子����,產(chǎn)生誤差
�;加入的KI必須過量的原因是除了與Cr(VI)充分反應(yīng)外�,還可以 保證實(shí)驗(yàn)的準(zhǔn)確性
保證實(shí)驗(yàn)的準(zhǔn)確性
���;
③產(chǎn)品中KCr(SO4)2?12H2O(M=499.0g/mol)的質(zhì)量分?jǐn)?shù)為 79.84%
79.84%
(保留4位有效數(shù)字)�。


